(Epi)genetyczne aspekty zespołu metabolicznego pa
obraz:
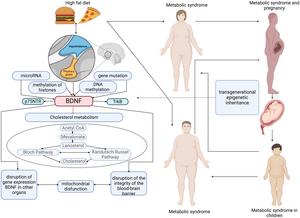
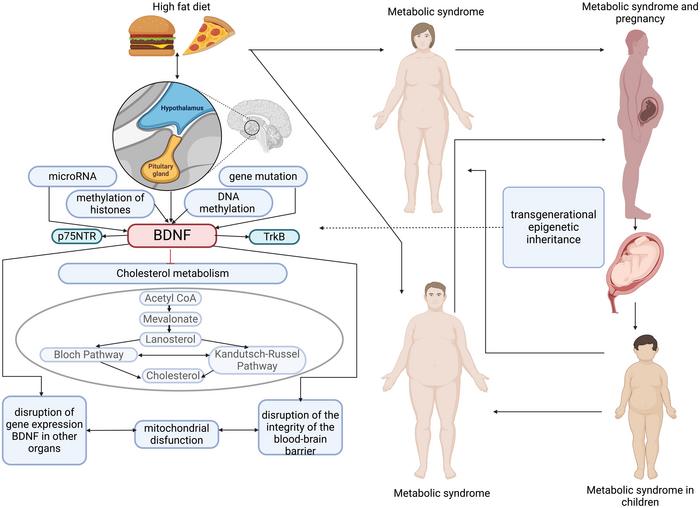
Dzieje się tak ze względu na składniki epigenetyczne: mikroRNA, metylację histonów i DNA, mutacje genów, które zmieniają ekspresję i produkcję czynnika neurotroficznego BDNF, który oddziałuje z receptorami p75NTR i TrkB. BDNF ma działanie regulujące na metabolizm cholesterolu w mózgu. Jednocześnie istnieje związek między zaburzeniem integralności bariery krew-mózg, ekspresją BDNF (również w innych narządach i tkankach) a dysfunkcją mitochondriów. Z drugiej strony dieta wysokokaloryczna i zespół metaboliczny u matek i ojców przyczyniają się do zaburzeń rozwoju płodu i predysponują potomstwo do rozwoju zespołu metabolicznego. Ten wzór jest wyjaśniony przez teorię dziedziczenia transgeneracyjnego, która wiąże zmiany w ekspresji BDNF z rozwojem chorób metabolicznych.BDNF, czynnik neurotroficzny pochodzenia mózgowego; p75NTR, receptor neurotrofiny p75; Acetylo-CoA, koenzym acetylowy; TrkB, receptor kinazy tropomiozyny B.
pogląd więcej
Źródło: Olga Khaziakhmatova, Natalia Todosenko
Zespół metaboliczny (MetS) to wieloaspektowe zaburzenie, które dotyka około 20–25% populacji świata. Zespół ten obejmuje szereg schorzeń, w tym otyłość, cukrzycę typu 2, hiperinsulinemię, insulinooporność (IR), hipercholesterolemię, niealkoholową stłuszczeniową chorobę wątroby, niealkoholowe stłuszczeniowe zapalenie wątroby i ogólnoustrojowe zapalenie metaboliczne. Stany te łącznie prowadzą do ciężkich chorób i zwiększonej przedwczesnej śmiertelności. Podwzgórze, krytyczna struktura mózgu regulująca zachowania żywieniowe, odgrywa kluczową rolę w rozwoju MetS. Związek między zaburzeniami psychoneurotycznymi a MetS podkreśla znaczącą rolę mózgu w postępie zespołu. Ponadto MetS jest związany z rozwojem raka, prawdopodobnie pośredniczonym przez dysfunkcję podwzgórza.
Podwzgórze jest integralną częścią homeostazy energetycznej i regulacji metabolizmu. Zapalenie i zmiany w funkcjonowaniu podwzgórza mogą wywołać zespół metaboliczny. W badaniach na zwierzętach dieta wysokotłuszczowa (HFD) u matek powoduje zapalenie podwzgórza i gliozę u potomstwa, przyczyniając się do dysregulacji metabolicznej. Integralność bariery krew-mózg (BBB) jest naruszona, co pozwala mediatorom zapalnym i kwasom tłuszczowym wpływać na rozwój podwzgórza płodu. Zmiany te prowadzą do zmian w komunikacji neuronalnej, zwiększonej ekspresji markerów zapalnych i zakłóceń w szlakach sygnałowych insuliny i leptyny, co sprzyja otyłości i insulinooporności u potomstwa.
Otyłość matki i ojca może epigenetycznie przeprogramować potomstwo, wpływając na jego zdrowie metaboliczne. Narażenie matki na HFD prowadzi do istotnych zmian w podwzgórzu potomstwa, w tym zwiększonej ekspresji genów związanych ze stanem zapalnym i zmienionym przekazem sygnałów neuronalnych. Zmiany te są zależne od płci, a potomstwo płci żeńskiej wykazuje większą podatność na zaburzenia metaboliczne. Otyłość ojca podobnie wpływa na potomstwo poprzez modyfikacje epigenetyczne, takie jak hipometylacja genów regulujących wzrost, przyczyniając się do dysfunkcji metabolicznych.
Dieta hiperkaloryczna matki wpływa na metabolizm lipidów i endogenny układ kannabinoidowy w podwzgórzu dorosłego potomstwa, co prowadzi do specyficznych dla płci reakcji metabolicznych. Dieta ta wywołuje wzrost ekspresji genów związanych z metabolizmem lipidów i receptorów kannabinoidowych w podwzgórzu. Takie zmiany zakłócają normalne procesy metaboliczne, przyczyniając się do rozwoju otyłości i innych zaburzeń metabolicznych u potomstwa.
Programowanie rozwojowe odgrywa kluczową rolę w określaniu podatności na zaburzenia metaboliczne. W krytycznych okresach rozwoju narażenie na niekorzystne czynniki środowiskowe, takie jak dieta hiperkaloryczna, może trwale zmienić strukturę i funkcję podwzgórza. Zmiany te predysponują jednostki do zaburzeń metabolicznych w późniejszym życiu. Mechanizmy epigenetyczne, w tym metylacja DNA i modyfikacje histonów, pośredniczą w tych długotrwałych efektach. Na przykład miRNA są kluczowe w regulacji rozwoju i funkcji podwzgórza, a na ich ekspresję wpływa dieta matki.
Podwzgórze zawiera kilka kluczowych szlaków sygnałowych, które regulują równowagę energetyczną i metabolizm. Na przykład szlak sygnałowy Notch bierze udział w neurogenezie podwzgórzowej i jest zaburzony u potomstwa otyłych matek, co prowadzi do zmienionego rozwoju neuronów i dysfunkcji metabolicznej. Podobnie, neurony POMC w podwzgórzu, które odgrywają kluczową rolę w regulacji apetytu i wydatkowania energii, są dotknięte otyłością matki i hiperglikemią, co skutkuje zwiększonym spożyciem pokarmu i przyrostem masy ciała u potomstwa.
Złożoność zespołu metabolicznego jest podkreślona przez skomplikowane współdziałanie czynników genetycznych, epigenetycznych i środowiskowych. Centralna rola podwzgórza w regulacji metabolizmu i znaczący wpływ otyłości rodzicielskiej na zdrowie metaboliczne potomstwa podkreślają znaczenie zajęcia się tymi czynnikami w celu złagodzenia rosnącej częstości występowania zespołu metabolicznego. Zrozumienie mechanizmów epigenetycznych i rozwojowych zaangażowanych w ten proces dostarcza wglądu w potencjalne cele terapeutyczne w zapobieganiu i leczeniu zaburzeń metabolicznych.
Pełny tekst
Badanie zostało niedawno opublikowane w Ekspresja genu.
Ekspresja genu (GE) to czasopismo o otwartym dostępie. Zostało uruchomione w 1991 r. przez Chicago Medical School Press, a w 1994 r. przeniesione do Cognizant Communication Corporation. Od sierpnia 2022 r. GE jest wydawane przez Xia & He Publishing Inc.
GE publikuje recenzowane i wysokiej jakości artykuły oryginalne, recenzje, artykuły redakcyjne, komentarze i opinie na temat głównych tematów badawczych, w tym biologii komórki, biologii molekularnej, genów i genetyki, w szczególności w zakresie komórkowych i molekularnych mechanizmów chorób człowieka.
GE zostało zaindeksowane w bazach Medline (1991-2021), Scopus, Biological Abstracts, Biosis Previews, ProQuest, itp.
Obserwuj nas na X: @xiahepublishing
Obserwuj nas na LinkedIn: Wydawnictwo Xia & He
Tytuł artykułu
(Epi)genetyczne aspekty patogenezy zespołu metabolicznego w odniesieniu do ekspresji czynnika neurotroficznego pochodzącego z mózgu: przegląd
Data publikacji artykułu
8-maj-2024
Zastrzeżenie: AAAS i EurekAlert! nie ponoszą odpowiedzialności za dokładność komunikatów prasowych zamieszczanych w EurekAlert! przez instytucje współpracujące, ani za sposób wykorzystania informacji za pośrednictwem systemu EurekAlert!