Immunoterapia obiecująca w leczeniu choroby Alzheimera
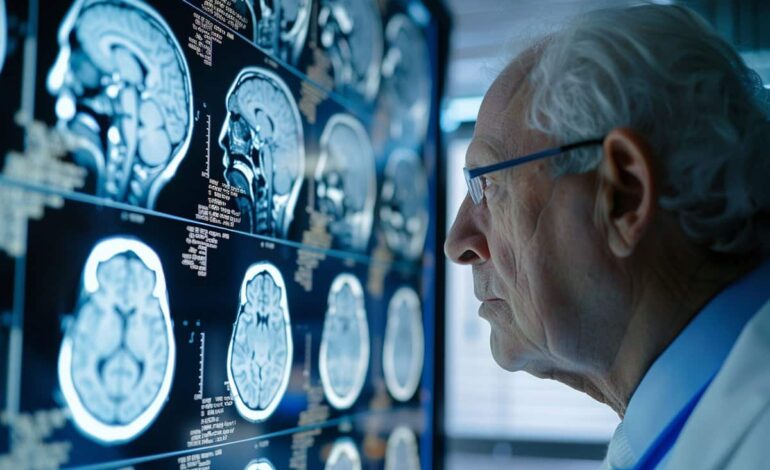
Streszczenie: Naukowcy zaprezentowali nowatorskie podejście do walki z chorobą Alzheimera poprzez aktywację mikrogleju, komórek odpornościowych mózgu, w celu pożerania płytek beta amyloidu, charakterystycznych dla tej choroby. Badanie to podkreśla potencjał stosowania immunoterapii nie tylko w leczeniu choroby Alzheimera, ale także innych chorób neurodegeneracyjnych charakteryzujących się szkodliwym nagromadzeniem białek.
Metoda opracowana przez zespół polega na użyciu przeciwciała w celu stymulacji mikrogleju do usuwania tych płytek, co stanowi obiecującą alternatywę dla obecnych metod leczenia, które są bezpośrednio ukierunkowane na beta-amyloid i mogą powodować działania niepożądane, takie jak ARIA. Ten przełom toruje drogę nowym strategiom terapeutycznym, które wykorzystują układ odpornościowy do walki z wyniszczającymi skutkami choroby Alzheimera i prawdopodobnie innych chorób, takich jak choroba Parkinsona i ALS.
Kluczowe fakty:
- Badanie wprowadza przełomową metodę aktywacji mikrogleju mózgu w celu usunięcia płytek amyloidowych beta, omijając bezpośrednie oddziaływanie na płytki obecnych leków na Alzheimera.
- Podejście to ma konsekwencje wykraczające poza chorobę Alzheimera i potencjalnie oferuje nowe możliwości leczenia szeregu chorób neurodegeneracyjnych charakteryzujących się toksycznymi grudkami białek.
- Chociaż istniejące metody leczenia, takie jak lekanemab, są obiecujące, niosą ze sobą ryzyko, takie jak ARIA, spowodowane usuwaniem amyloidu z naczyń krwionośnych mózgu; nowa metoda stanowi potencjalnie bezpieczniejszą alternatywę.
Źródło: WUSTL
Choroba Alzheimera zaczyna się od lepkiego białka zwanego amyloidem beta, które gromadzi się w blaszkach w mózgu, rozpoczynając łańcuch zdarzeń prowadzący do zaniku mózgu i pogorszenia funkcji poznawczych.
Nowa generacja leków na Alzheimera – pierwszych, o których udowodniono, że zmieniają przebieg choroby – działa poprzez znakowanie amyloidu w celu usunięcia go przez komórki odpornościowe mózgu.
Teraz naukowcy z Washington University School of Medicine w St. Louis znaleźli inny i obiecujący sposób usuwania szkodliwych płytek: poprzez bezpośrednią mobilizację komórek odpornościowych do ich spożycia.
W badaniu opublikowanym 3 kwietnia br Naukowa medycyna translacyjnanaukowcy wykazali, że aktywacja komórek odpornościowych zwanych mikroglejem za pomocą przeciwciała zmniejsza blaszki amyloidowe w mózgu i łagodzi zaburzenia behawioralne u myszy chorych na chorobę Alzheimera.
Podejście to może mieć konsekwencje wykraczające poza chorobę Alzheimera. Toksyczne skupiska białek mózgowych są cechą wielu schorzeń neurodegeneracyjnych, w tym choroby Parkinsona, stwardnienia zanikowego bocznego (ALS) i choroby Huntingtona.
Zachęceni wynikami badania naukowcy badają inne potencjalne immunoterapie – leki ujarzmiające układ odpornościowy – w celu usunięcia z mózgu zbędnych białek, które, jak się uważa, powodują rozwój innych chorób.
„Ogólnie aktywując mikroglej, nasze przeciwciało może usuwać płytki beta amyloidu u myszy i może potencjalnie usuwać inne szkodliwe białka w innych chorobach neurodegeneracyjnych, w tym w chorobie Parkinsona” – wyjaśnił starszy autor badania, lekarz medycyny Marco Colonna, Robert Rock Belliveau, MD, profesor patologii.
Mikroglej otacza płytki, tworząc barierę kontrolującą rozprzestrzenianie się szkodliwego białka. Mogą również pochłaniać i niszczyć białka płytki nazębnej, ale w chorobie Alzheimera zwykle tego nie robią. Źródłem ich bierności może być białko zwane APOE, będące składnikiem płytek amyloidowych.
Białka APOE w płytce wiążą się z receptorem – LILRB4 – na mikrogleju otaczającym płytki, dezaktywując je, wyjaśnia Yun Chen, współautor badania.
Z wciąż nieznanych powodów naukowcy odkryli, że u myszy i osób chorych na chorobę Alzheimera mikroglej otaczający płytki wytwarza i umieszcza LILRB4 na powierzchni komórek, co hamuje ich zdolność do kontrolowania tworzenia szkodliwych płytek po związaniu się z APOE.
Drugi współautor, dr Jinchao Hou, obecnie pracownik naukowy Szpitala Dziecięcego Szkoły Medycznej Uniwersytetu Zhejiang w prowincji Zhejiang w Chinach, leczył myszy, które miały w mózgu blaszki beta amyloidu, domowym przeciwciałem, które blokowało wiązanie się APOE z LILRB4.
Po współpracy z doktorem Yongjianem Liu, profesorem radiologii w Instytucie Radiologii Mallinckrodt na Uniwersytecie Waszyngtońskim, w celu potwierdzenia, że przeciwciało dotarło do mózgu, naukowcy odkryli, że aktywowany mikroglej jest w stanie wchłonąć i usunąć blaszki beta amyloidu.
Usuwanie płytek beta amyloidu u myszy łagodzi również ryzykowne zachowania. Osobom z AD może brakować pamięci o przeszłych doświadczeniach, która pomagałaby im w podejmowaniu decyzji.
Mogą angażować się w ryzykowne zachowania, przez co mogą stać się ofiarami oszustwa lub nadużyć finansowych. Leczenie myszy przeciwciałem w celu usunięcia płytek okazało się obiecujące w zakresie zmiany zachowania.
Po utworzeniu się płytek beta amyloidu w mózgu inne białko mózgowe – tau – zostaje splątane w neuronach. W tym drugim stadium choroby neurony obumierają i pojawiają się objawy poznawcze. Chen wyjaśnił, że u pacjentów z AD na tym późniejszym etapie zaobserwowano wysoki poziom LILRB4 i APOE.
Możliwe, że zablokowanie interakcji białek i aktywacji mikrogleju może zmienić późniejsze stadia choroby. W przyszłych badaniach naukowcy będą testować przeciwciało na myszach ze splątkami tau.
Leki działające bezpośrednio na płytki amyloidowe mogą powodować potencjalnie poważne skutki uboczne. U pacjentów z chorobą Alzheimera białka amyloidowe gromadzą się na ścianach tętnic w mózgu, a także w innych częściach tkanki mózgowej. Usunięcie blaszek z naczyń krwionośnych mózgu może wywołać obrzęk i krwawienie, efekt uboczny znany jako ARIA.
To działanie niepożądane obserwuje się u niektórych pacjentów otrzymujących lekanemab – lek zatwierdzony przez Agencję ds. Żywności i Leków do leczenia choroby Alzheimera. Myszy użyte w tym badaniu nie posiadały płytek amyloidowych na naczyniach krwionośnych, dlatego badacze nie byli w stanie ocenić, co się stanie po usunięciu płytek amyloidowych.
Pracują z innym modelem myszy – takim, który rzeczywiście ma blaszki w tętnicach mózgowych – aby zrozumieć, czy to nowe podejście niesie również ryzyko ARIA.
„Lekanemab, jako pierwsze przeciwciało terapeutyczne, które było w stanie zmodyfikować przebieg choroby, potwierdził znaczenie białka beta amyloidu w postępie choroby Alzheimera” – powiedział autor David Holtzman, lekarz medycyny, Barbara Burton i Reuben M. Morriss III Distinguished Profesor neurologii.
„Otworzyło to nowe możliwości opracowania innych immunoterapii wykorzystujących różne metody usuwania szkodliwych białek z mózgu”.
O tej immunoterapii i nowościach badawczych nad chorobą Alzheimera
Autor: Marta Węgorzewska
Źródło: WUSTL
Kontakt: Marta Węgorzewska – WUSTL
Obraz: Zdjęcie przypisuje się Neuroscience News
Orginalne badania: Zamknięty dostęp.
„Za pośrednictwem przeciwciał kierowanie na ludzki receptor Ig-podobny z ludzkich leukocytów mikrogleju B4 osłabia patologię amyloidu w modelu mysim” – David Holtzman i in. Naukowa medycyna translacyjna
Abstrakcyjny
Celowanie za pośrednictwem przeciwciał w ludzki receptor Ig-podobny B4 leukocytów mikrogleju osłabia patologię amyloidu w modelu mysim
Mikroglej pomaga ograniczyć postęp choroby Alzheimera (AD) poprzez ograniczenie patologii amyloidu-β (Aβ), na co wpływa równowaga aktywujących i hamujących sygnałów wewnątrzkomórkowych dostarczanych przez różne receptory na powierzchni komórki.
Ludzki receptor leukocytowy Ig-podobny B4 (LILRB4) jest receptorem hamującym z nadrodziny immunoglobulin (Ig), który ulega ekspresji na komórkach szpikowych i rozpoznaje między innymi apolipoproteinę E (ApoE).
Tutaj stwierdzamy, że LILRB4 ulega silnej ekspresji w mikrogleju pacjentów z AD. Używając myszy, które akumulują Aβ i niosą transgen obejmujący część LILR region, który obejmuje LILRB4potwierdziliśmy obfitą ekspresję LILRB4 w mikrogleju owijającym się wokół płytek Aβ.
Ogólnoustrojowe leczenie tych myszy przeciwciałem monoklonalnym (mAb) skierowanym przeciwko ludzkiemu LILRB4 zmniejszyło obciążenie Aβ, złagodziło niektóre nieprawidłowości behawioralne związane z Aβ, zwiększyło aktywność mikrogleju i osłabiło ekspresję genów indukowanych interferonem.
Eksperymenty z wiązaniem in vitro wykazały, że ludzki LILRB4 wiąże zarówno ludzką, jak i mysią ApoE i że mAb anty-ludzkie LILRB4 blokuje taką interakcję.
Modelowanie in silico, analizy biochemiczne i mutagenezy zidentyfikowały pętlę pomiędzy dwiema zewnątrzkomórkowymi domenami Ig LILRB4 wymaganymi do interakcji z mysim ApoE i ponadto wskazały, że mAb anty-LILRB4 może blokować LILRB4-mApoE poprzez bezpośrednie wiązanie tej pętli. Zatem ukierunkowanie na LILRB4 może być potencjalną drogą terapeutyczną w przypadku AD.






