MikroRNA jest głównym regulatorem genomu — badacze uczą się, jak wykorzystać sposób, w jaki kontroluje on geny
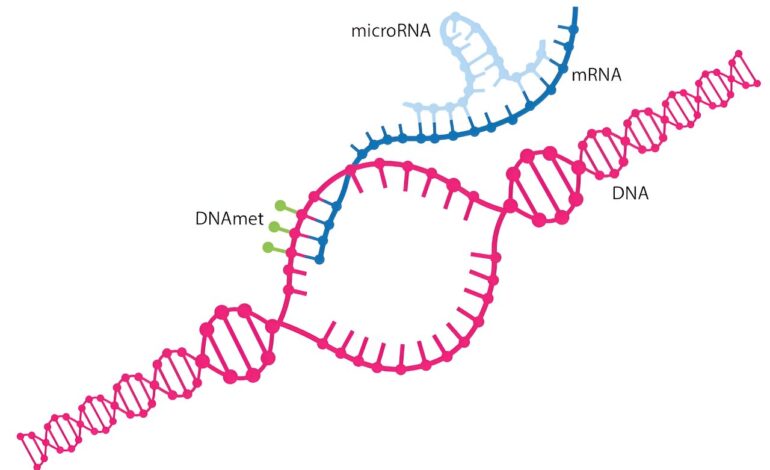
Ziemia powstała 4,5 miliarda lat temu, a życie niecałe miliard lat później. Chociaż życie, jakie znamy, zależy od czterech głównych makrocząsteczek – DNA, RNA, białek i lipidów – uważa się, że tylko jedna była obecna na początku życia: RNA.
Nic dziwnego, że najprawdopodobniej na pierwszym miejscu znalazło się RNA. Jest to jedyna z głównych makrocząsteczek, która może zarówno replikować się, jak i katalizować reakcje chemiczne, które są niezbędne do życia. Podobnie jak DNA, RNA składa się z pojedynczych nukleotydów połączonych w łańcuchy. Naukowcy początkowo zrozumieli, że informacja genetyczna przepływa w jednym kierunku: DNA ulega transkrypcji na RNA, a RNA ulega translacji na białka. Zasada ta nazywana jest centralnym dogmatem biologii molekularnej. Ale jest wiele odchyleń.
Jednym z głównych przykładów wyjątku od głównego dogmatu jest to, że niektóre RNA nigdy nie ulegają translacji ani kodowaniu w białka. To fascynujące odejście od głównego dogmatu skłoniło mnie do poświęcenia mojej kariery naukowej zrozumieniu, jak to działa. Rzeczywiście, badania nad RNA pozostają w tyle za innymi makrocząsteczkami. Chociaż istnieje wiele klas tak zwanych niekodujących RNA, badacze tacy jak ja zaczęli skupiać dużą uwagę na krótkich odcinkach materiału genetycznego zwanych mikroRNA i ich potencjale w leczeniu różnych chorób, w tym raka.
MikroRNA i choroby
Naukowcy uważają mikroRNA za główne regulatory genomu ze względu na ich zdolność do wiązania się i zmiany ekspresji wielu RNA kodujących białka. Rzeczywiście, pojedynczy mikroRNA może regulować od 10 do 100 RNA kodujących białka. Zamiast tłumaczyć DNA na białka, zamiast tego mogą wiązać się z RNA kodującymi białka, aby wyciszyć geny.
Powód, dla którego mikroRNA mogą regulować tak zróżnicowaną pulę RNA, wynika z ich zdolności do wiązania się z docelowymi RNA, z którymi nie pasują idealnie. Oznacza to, że pojedynczy mikroRNA często może regulować pulę celów, z których wszystkie biorą udział w podobnych procesach w komórce, co prowadzi do wzmocnionej odpowiedzi.
Ponieważ pojedynczy mikroRNA może regulować wiele genów, wiele mikroRNA może przyczyniać się do chorób, gdy staną się dysfunkcjonalne.
W 2002 roku badacze po raz pierwszy zidentyfikowali rolę, jaką odgrywają dysfunkcjonalne mikroRNA w chorobach pacjentów cierpiących na rodzaj raka krwi i szpiku kostnego zwany przewlekłą białaczką limfatyczną. Rak ten wynika z utraty dwóch mikroRNA normalnie zaangażowanych w blokowanie wzrostu komórek nowotworowych. Od tego czasu naukowcy zidentyfikowali u ludzi ponad 2000 mikroRNA, z których wiele ulega zmianom w wyniku różnych chorób.
W tej dziedzinie udało się również uzyskać dość solidną wiedzę na temat wpływu dysfunkcji mikroRNA na choroby. Zmiana jednego mikroRNA może spowodować zmianę kilku innych genów, co skutkuje mnóstwem zmian, które łącznie mogą zmienić fizjologię komórki. Na przykład ponad połowa wszystkich nowotworów ma znacznie zmniejszoną aktywność w mikroRNA zwanym miR-34a. Ponieważ miR-34a reguluje wiele genów zaangażowanych w zapobieganie wzrostowi i migracji komórek nowotworowych, utrata miR-34a może zwiększyć ryzyko zachorowania na raka.
Naukowcy rozważają wykorzystanie mikroRNA w leczeniu raka, chorób serca, chorób neurodegeneracyjnych i innych. Chociaż wyniki laboratoryjne były obiecujące, wprowadzenie terapii mikroRNA do kliniki napotkało wiele wyzwań. Wiele z nich wiąże się z nieefektywnym dostarczaniem do komórek docelowych i słabą stabilnością, co ogranicza ich skuteczność.
Dostarczanie mikroRNA do komórek
Jednym z powodów, dla których dostarczanie terapii mikroRNA do komórek jest trudne, jest to, że leczenie mikroRNA musi być dostarczane konkretnie do chorych komórek, unikając zdrowych komórek. W przeciwieństwie do szczepionek mRNA przeciwko COVID-19, które są pobierane przez oczyszczanie komórek odpornościowych, których zadaniem jest wykrywanie obcych materiałów, leczenie mikroRNA musi oszukać organizm, aby myślał, że nie są one obce, aby uniknąć ataku immunologicznego i dotrzeć do docelowych komórek.
Naukowcy badają różne sposoby dostarczania terapii mikroRNA do konkretnych komórek docelowych. Jedna z metod cieszących się dużym zainteresowaniem polega na bezpośrednim połączeniu mikroRNA z ligandem, rodzajem małej cząsteczki, która wiąże się z określonymi białkami na powierzchni komórek. W porównaniu ze zdrowymi komórkami, chore komórki mogą mieć nieproporcjonalną liczbę niektórych białek powierzchniowych, czyli receptorów. Zatem ligandy mogą pomóc mikroRNA dotrzeć do chorych komórek, unikając jednocześnie zdrowych komórek. Pierwszy ligand zatwierdzony przez amerykańską Agencję ds. Żywności i Leków do dostarczania małych RNA, takich jak mikroRNA, N-acetylogalaktozamina lub GalNAc, preferencyjnie dostarcza RNA do komórek wątroby.
Identyfikacja ligandów, które mogą dostarczać małe RNA do innych komórek, wymaga znalezienia receptorów ulegających ekspresji na wystarczająco wysokim poziomie na powierzchni komórek docelowych. Zazwyczaj, aby zapewnić wystarczające dostarczenie leku, potrzebnych jest ponad milion kopii na komórkę.
Jednym z wyróżniających się ligandów jest kwas foliowy, określany również jako witamina B9, mała cząsteczka krytyczna w okresach szybkiego wzrostu komórek, takich jak rozwój płodu. Ponieważ niektóre komórki nowotworowe mają ponad milion receptorów kwasu foliowego, ligand ten zapewnia wystarczającą możliwość dostarczenia wystarczającej ilości terapeutycznego RNA, aby celować w różne typy nowotworów. Na przykład moje laboratorium opracowało nową cząsteczkę o nazwie FolamiR-34a – folian powiązany z miR-34a – która zmniejszała wielkość nowotworów piersi i płuc u myszy.
Zwiększanie stabilności mikroRNA
Jednym z innych wyzwań związanych ze stosowaniem małych RNA jest ich słaba stabilność, co prowadzi do ich szybkiej degradacji. W związku z tym terapie oparte na RNA są na ogół krótkotrwałe w organizmie i wymagają częstych dawek, aby utrzymać efekt terapeutyczny.
Aby przezwyciężyć to wyzwanie, badacze na różne sposoby modyfikują małe RNA. Chociaż każdy RNA wymaga określonego wzorca modyfikacji, udane zmiany mogą znacznie zwiększyć jego stabilność. Zmniejsza to potrzebę częstego dawkowania, co w konsekwencji zmniejsza obciążenie i koszty leczenia.
Na przykład zmodyfikowane GalNAc-siRNA, inna forma małych RNA, w komórkach niedzielących się zmniejszają dawkowanie z co kilka dni do raz na sześć miesięcy. Mój zespół opracował ligandy kwasu foliowego połączone ze zmodyfikowanymi mikroRNA do leczenia raka, w ramach których zmniejszono dawkowanie z raz na drugi dzień do raz w tygodniu. W przypadku chorób takich jak rak, w których komórki szybko się dzielą i szybko rozcieńczają dostarczone mikroRNA, ten wzrost aktywności stanowi znaczący postęp w tej dziedzinie. Przewidujemy, że to osiągnięcie ułatwi dalszy rozwój tego mikroRNA połączonego z kwasem foliowym jako metody leczenia raka w nadchodzących latach.
Chociaż nadal pozostaje wiele do zrobienia, aby pokonać przeszkody związane z leczeniem mikroRNA, jasne jest, że RNA jest obiecującym środkiem terapeutycznym w przypadku wielu chorób.