Narzędzia pomagające naukowcom zwiększyć tempo znajdowania nowych leków
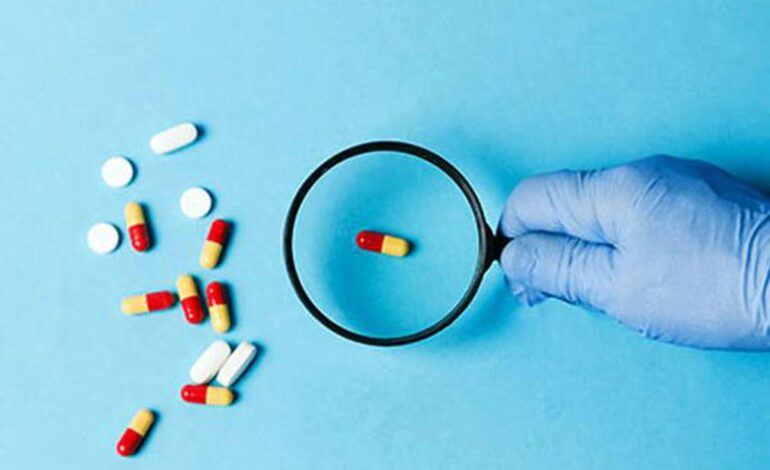
Indie są jednym z wiodących na świecie producentów i konsumentów leków przeciwdrobnoustrojowych. Jednak wiele z tych ratujących życie leków staje się obecnie nieskutecznych w walce z bakteriami chorobotwórczymi. W 2019 r. z powodu nieskutecznych leków przeciwdrobnoustrojowych na całym świecie zmarło około 4,9 mln ludzi. Do zgonów tych zaliczają się zgony spowodowane infekcjami, a także zachorowania wynikające z oporności na środki przeciwdrobnoustrojowe. Jednak wciąż mamy trudności ze znalezieniem nowych leków.
Jednym ze sposobów wyjścia z tego kryzysu jest odkrycie przez badaczy nowych szlaków kluczowych dla przetrwania patogenów i zakłócenie ich. Jednakże nowoczesny proces odkrywania ukierunkowanych leków jest procesem złożonym i często wymaga rozwiązań dostosowanych do każdego celu.
Jak zaczyna się odkrywanie leków?
Dwie grupy badawcze pracujące w CSIR-Centrum Biologii Komórkowej i Molekularnej w Hyderabadzie zidentyfikowały niedawno potencjalne cele dla nowych leków przeciwmalarycznych, badając podstawową biologię Escherichia coli bakteriami i ludzkim pasożytem malarii Plasmodium falciparum.
Grupa Manjuli Reddy badała, w jaki sposób zewnętrzne ściany komórkowe bakterii rozszerzają się, gdy komórka bakteryjna rośnie, zanim podzieli się na dwie części. Grupa koncentruje się na warstwie peptydoglikanu, siatce cukru i aminokwasów E coli niezbędne do przeżycia bakterii. Kiedy komórka rośnie, siatka pęka i dodaje się dodatkowy materiał peptydoglikanowy w celu powiększenia siatki.
W ciągu ostatniej dekady grupa dr Reddy’ego zidentyfikowała zestaw enzymów hydrolazy peptydoglikanu odpowiedzialnych za przecinanie warstwy peptydoglikanu, a najnowszy opublikowany w czasopiśmie Genetyka PLoS w lutym. Enzymy te są obecne we wszystkich typach bakterii i są silnymi celami leków. Zahamowanie ich może zapobiec rozszerzaniu się warstwy peptydoglikanu, a tym samym zabiciu bakterii.
Podobnie grupa Purana Singha Sijwali bada, w jaki sposób P. falciparum pasożyt rośnie w ludzkich czerwonych krwinkach i komórkach wątroby, w zależności od etapu rozwoju. Grupa skupia się na tym, jak pasożyt rozkłada własne białka, których już nie potrzebuje. Wykorzystuje klasę enzymów zwanych ligazami Cullin RING. Oznaczają białka innym małym białkiem zwanym ubikwityną. Aparat do degradacji białek identyfikuje ubikwitynę i rozbija białko, do którego jest przyłączona ubikwityna.
Niedawno grupa dr Sijwali opisała w czasopiśmie dwa takie enzymy kluczowe dla rozwoju pasożyta Patogeny PLoS.
Z ilu etapów składa się odkrywanie?
Następnym krokiem dla nich jest znalezienie leków, które będą działać na te zidentyfikowane cele. Jednak szybkie przeszukanie bazy danych PubMed (zawierającej artykuły z zakresu nauk przyrodniczych i badań biomedycznych) pokazuje, że naukowcy na całym świecie publikują tysiące artykułów opisujących nowe cele leków – choć większość z nich nie została jeszcze przełożona na nowe leki.
Główną przyczyną istnienia bariery jest potrzeba współpracy osób posiadających wiedzę specjalistyczną w różnych obszarach przez dłuższy okres czasu.

Zwykle proces odkrywania leku rozpoczyna się od znalezienia cząsteczki inhibitora, która wiąże się z celem i blokuje jego działanie. Naukowcy sprawdzają, jak dobrze obie cząsteczki łączą się ze sobą, co zależy od ich struktury i właściwości chemicznych. Doktor Reddy opracowała prosty i solidny test, który pozwala jej zwizualizować, czy cząsteczki podobne do leku działają na docelowe enzymy. Jednak większość naukowców potrzebuje dostępu do struktur potencjalnych celów leków, aby posunąć prace do przodu.
Z którym współpracuje dr Reddy E coli, organizm modelowy. Wiele struktur białkowych E coli są już dostępne w bazach danych. Nie dotyczy to jednak prac dr Sijwali i innych: określenie struktury enzymów, nad którymi pracowali, jest trudne, ponieważ są to duże cząsteczki zbudowane z wielu białek (każde zawierające ponad 20 000 atomów).
Jak inaczej można ujawnić struktury enzymów?
Kolejną najlepszą rzeczą jest ocena struktury enzymu w oparciu o znane struktury podobnych cząsteczek, zwanych homologami, w innych organizmach. Im bardziej ewolucyjnie spokrewnione są homologi, tym bardziej podobne będą ich struktury.
Następnie naukowcy analizują struktury cząsteczek docelowych za pomocą programów komputerowych zwanych symulacjami dokowania molekularnego. Programy te próbują dopasować znane struktury małych związków lekopodobnych do struktury cząsteczki docelowej i przewidzieć, jak dobrze będą się one ze sobą wiązać. Pomocna jest dostępność wielu takich bibliotek chemicznych.
Istnieją biblioteki leków zatwierdzonych już przez agencje, takie jak amerykańska Agencja ds. Żywności i Leków, ze względu na ich bezpieczeństwo, a wiele z nich jest już sprzedawanych na rynku w związku z chorobą. Istnieją również znacznie większe biblioteki związków chemicznych, które instytuty badawcze stworzyły i/lub zidentyfikowały jako skuteczne w walce z interesującą ich chorobą, ale które nie zostały jeszcze przetestowane pod kątem bezpieczeństwa u ludzi.
Czy sztuczna inteligencja może pomóc?
Tam, gdzie istniejące biblioteki również nie spełniają swoich oczekiwań, niektóre programy komputerowe oparte na sztucznej inteligencji mogą również przewidywać struktury potencjalnych cząsteczek leków. Chemicy potrafią je zsyntetyzować od nowa (od zera) lub można wybrać istniejące cząsteczki o podobnych strukturach i zmodyfikować je.
Niektórzy, jak dr Sijwali, wnoszą swoją wiedzę specjalistyczną do firm wykorzystujących sztuczną inteligencję, aby pomóc w obliczeniowym odkrywaniu leków, i planują współpracować z przemysłem farmaceutycznym w celu ich syntezy.
Inni zalecają, aby firmy farmaceutyczne dodały nowo odkryte cele do swoich list produktów do przetestowania. Firmy te mają już możliwość przeprowadzania wysokowydajnych badań przesiewowych – procesu, w którym badacze sprawdzają równolegle przydatność tysięcy, a nawet milionów cząsteczek. Takie cząsteczki są bardziej wykonalne pod względem logistycznym i finansowym niż jeden naukowiec testujący kilka celów dla leków.

Dlaczego odkrywanie leków jest wyzwaniem?
Po zidentyfikowaniu odpowiedniej grupy cząsteczek należy je poddać proceduralnym testom pod kątem bezpieczeństwa i skuteczności. Najpierw w modelu hodowli komórkowej, a następnie w eksperymentalnych modelach zwierzęcych badacze sprawdzają, czy inhibitory działają selektywnie przeciwko patogenom (a nie przeciwko komórkom ludzkim). Dziś wiele startupów pracuje także jako kontraktowe laboratoria badawcze i przeprowadza takie testy. Następnie rozpoczynają się badania kliniczne, które są ściśle regulowane, aby zapewnić ich etyczne prowadzenie i uzyskanie danych nienaruszonych przez jakiekolwiek uprzedzenia. Jeśli wyniki prób przekroczą z góry ustalony próg sukcesu, organy regulacyjne zatwierdzają leki na rynek.
Droga pomiędzy zidentyfikowaniem nowych celów dla narkotyków a faktycznym posiadaniem leków przeciwko tym celom jest długa, ale konieczna. Aby ułatwić ten proces, wymagana jest różnego rodzaju wiedza specjalistyczna. Opracowywanie narzędzi, takich jak symulacje dokowania molekularnego, odkrywanie leków w oparciu o sztuczną inteligencję i biblioteki chemiczne, stanowi przykład współpracy między biologami zajmującymi się chorobami zakaźnymi, biologami strukturalnymi, biologami obliczeniowymi, chemikami i różnymi instytucjami badawczymi motywowanymi wspólną przyczyną i, oczywiście, wystarczającym finansowaniem. Sieć ta również musi zostać rozszerzona, aby objąć start-upy i całą branżę.
Naukowcy dokonują bardziej fundamentalnych odkryć dotyczących patogenów, które są istotne dla większej liczby społeczności lokalnych — P. falciparum lub Mycobacterium tuberculosis w Azji Południowej, np. społeczność badawczo-innowacyjna w tych regionach powinna zwrócić na nie uwagę, połączyć siły i wykorzystać najlepsze dostępne techniki i obiekty w celu przyspieszenia odkrywania leków.
Doktor Somdatta Karak jest kierownikiem ds. komunikacji naukowej w CSIR-Centrum Biologii Komórkowej i Molekularnej w Hyderabadzie.
To jest artykuł Premium dostępny wyłącznie dla naszych subskrybentów. Aby czytać ponad 250 takich artykułów premium każdego miesiąca
Wyczerpałeś limit bezpłatnych artykułów. Prosimy o wsparcie dobrego dziennikarstwa.
Wyczerpałeś limit bezpłatnych artykułów. Prosimy o wsparcie dobrego dziennikarstwa.
Przeczytałeś {{data.cm.views}} poza {{data.cm.maxViews}} darmowe artykuły.
To jest Twój ostatni darmowy artykuł.






