Naukowcy odkrywają nowatorski nośnik antybiotyku
obraz:
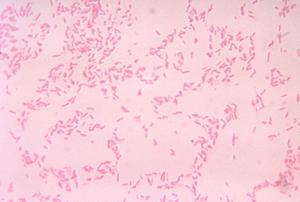
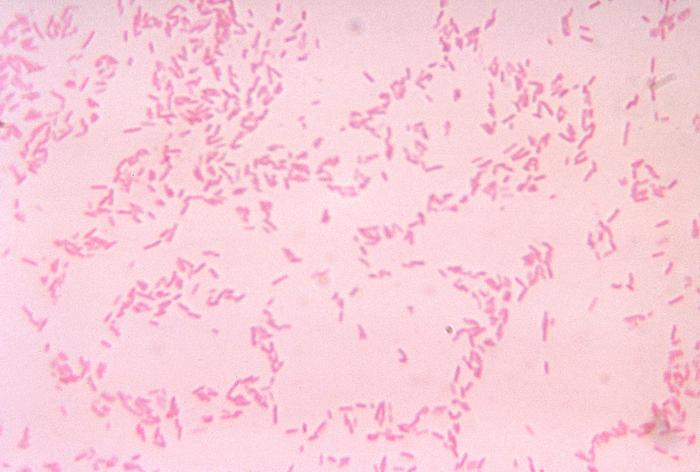
B. fragilis to bakteria komensalna, która normalnie żyje w przewodzie pokarmowym człowieka. Może stać się patogenny w wyniku uszkodzenia normalnej błony śluzowej jelit w wyniku urazu lub operacji. Źródło: Centra Kontroli Chorób/VR Dowell Jr.
pogląd więcej
Źródło: Źródło: Centra Kontroli Chorób/VR Dowell Jr.
Autor: David L. Chandler
WOODS HOLE, Massachusetts — Oporność na antybiotyki jest znaczącym i narastającym problemem medycznym na całym świecie. Naukowcy z Marine Biological Laboratory (MBL) i współpracownicy odkryli nowy układ genetyczny, który może pomóc powszechnej bakterii w ludzkich jelitach, Bacteroides fragilischronić się przed tetracykliną, powszechnie stosowanym antybiotykiem.
Chociaż odkrycia te nie doprowadzą bezpośrednio do nowych sposobów zwalczania bakterii opornych na tetracykliny, naukowcy odkryli niewidziane wcześniej układy genetyczne nadające oporność na antybiotyki. Takie zrozumienie może pomóc w opracowaniu nowych sposobów ograniczania rozprzestrzeniania się genów oporności na antybiotyki poprzez manipulację genetyczną lub inne środki.
O odkryciach poinformowano w czasopiśmie mBio przez naukowców z MBL Josepha Vineisa, Mitchella Sogina i Blaira Paula wraz z kolegami z MBL, Argonne National Laboratory i University of Chicago.
Badane przez nich bakterie Bacteroides fragilis, wyizolowano od pacjenta z wrzodziejącym zapaleniem jelita grubego, u którego stwierdzono jego obfitość w okresach stanu zapalnego. Zespół miał do analizy duży zestaw próbek od pacjentów z nieswoistym zapaleniem jelit, którzy byli leczeni chirurgicznie w celu złagodzenia stanu zapalnego.
Próbki te badano w MBL przy użyciu metagenomiki typu shotgun, która pozwala uzyskać sekwencje całego materiału genetycznego w całej społeczności komórek drobnoustrojów. Ułatwia także hodowlę szczepów bakteryjnych pochodzących ze społeczności, dostarczając danych niezbędnych do obserwacji aktywności genów oporności na tetracyklinę podczas wzrostu w obecności tetracykliny. (W czasie, gdy rozpoczynali tę pracę, mówi Vineis, „możliwość rekonstrukcji genomów na podstawie danych metagenomicznych była dopiero początkiem w terenie. Było to nowatorskie podejście, ale obecnie jest powszechne”.)
„Kiedy spojrzeliśmy na dane” – mówi Vineis – „był bardzo silny sygnał” wskazujący na dużą liczbę kopii poszczególnych regionów genomu bakterii. Jeden z tych regionów, obejmujący wiele genów, „był bardzo obfity” w próbce, a później udało im się ustalić, „że ten konkretny region o dużej liczbie kopii zawierał oporność na tetracyklinę… Więc kopaliśmy dalej”.
Te licznie kopiowane sekcje genomu zawierały fragmenty DNA, które mogą przemieszczać się w genomie, a nawet przeskakiwać do innego genomu. Te mobilne elementy genetyczne, zwane transpozonami, stanowią „ważny sposób, w jaki bakterie mogą przystosować się do środowiska bez konieczności całkowitego ich wymyślania na nowo” – mówi Vineis. Natomiast w jelitach człowieka, gdzie stale blisko siebie znajduje się ogromna liczba gatunków bakterii jelitowych, „potencjał wymiany jest naprawdę wysoki” – mówi, a współczynnik ten wzrasta w przypadku stanu zapalnego.
Taka wymiana materiału genetycznego pomiędzy różnymi gatunkami nazywana jest transferem poziomym. Blair Paul, asystent naukowy w MBL, mówi, że „uważamy, że te transpozony są w rzeczywistości kluczowym nośnikiem horyzontalnego transferu genów”.
W tym przypadku bakterie najwyraźniej wyczuwają obecność tetracykliny w środowisku i rozpoczynają „całą kaskadę” produkcji transpozonu zawierającego gen oporności, mówi Vineis.
Odkryli, że część transpozonu zawierająca gen oporności występuje w dwóch różnych postaciach w tym samym genomie: czasami ma normalną postać liniową, a czasami jest zwinięta w okrąg. Obie formy występują jednocześnie w Bacteroides fragilis genomu, ale postać liniowa zawiera unikalną wstawkę genomową w regionie DNA, która koduje maszynerię mobilizacji do innych komórek.
„O ile nam wiadomo, nie zaobserwowano tego wcześniej” – mówi Paul – „ten konkretny typ transpozonu ma wzmocniony podregion. Dzieje się tak u bakterii, które współwystępują ze stanem zapalnym.”
Zwiększona ekspresja tej grupy genów jest potencjalnie powiązana z sukcesem Bacteroides fragilis podczas stanu zapalnego, chociaż związek nie został jeszcze udowodniony i wymaga dalszych badań. Paul twierdzi jednak, że odkrycia „rodzą nowe pytania dotyczące roli transferu genów dla zdrowia ludzkiego, ale także tego, w jaki sposób transpozony są kontrolowane i jak mogą zmieniać się ewolucyjnie w czasie”.
„To odkrycie nie zmieni naszego zrozumienia świata oporności na antybiotyki, ale jest to nowatorski mechanizm, którego przynajmniej możemy zacząć szukać” – mówi Vineis. „W świecie drobnoustrojów ma miejsce wiele ataków i obrony, z których nawet nie jesteśmy w pełni świadomi”.
—###—
The Morskie Laboratorium Biologiczne (MBL) zajmuje się odkryciami naukowymi – badaniem biologii podstawowej, zrozumieniem różnorodności biologicznej morza i środowiska oraz informowaniem o kondycji człowieka poprzez badania i edukację. Założona w Woods Hole w stanie Massachusetts w 1888 roku MBL jest prywatną instytucją non-profit i stowarzyszoną z Uniwersytet w Chicago.
Metoda badań
Analiza danych/statystyczna
Tytuł artykułu
Nowatorski transpozon koniugacyjny niosący autonomicznie amplifikowany plazmid
Data publikacji artykułu
23 stycznia 2024 r
Zastrzeżenie: AAAS i EurekAlert! nie odpowiadają za dokładność komunikatów prasowych publikowanych w EurekAlert! przez instytucje wnoszące wkład lub za wykorzystanie jakichkolwiek informacji za pośrednictwem systemu EurekAlert.






