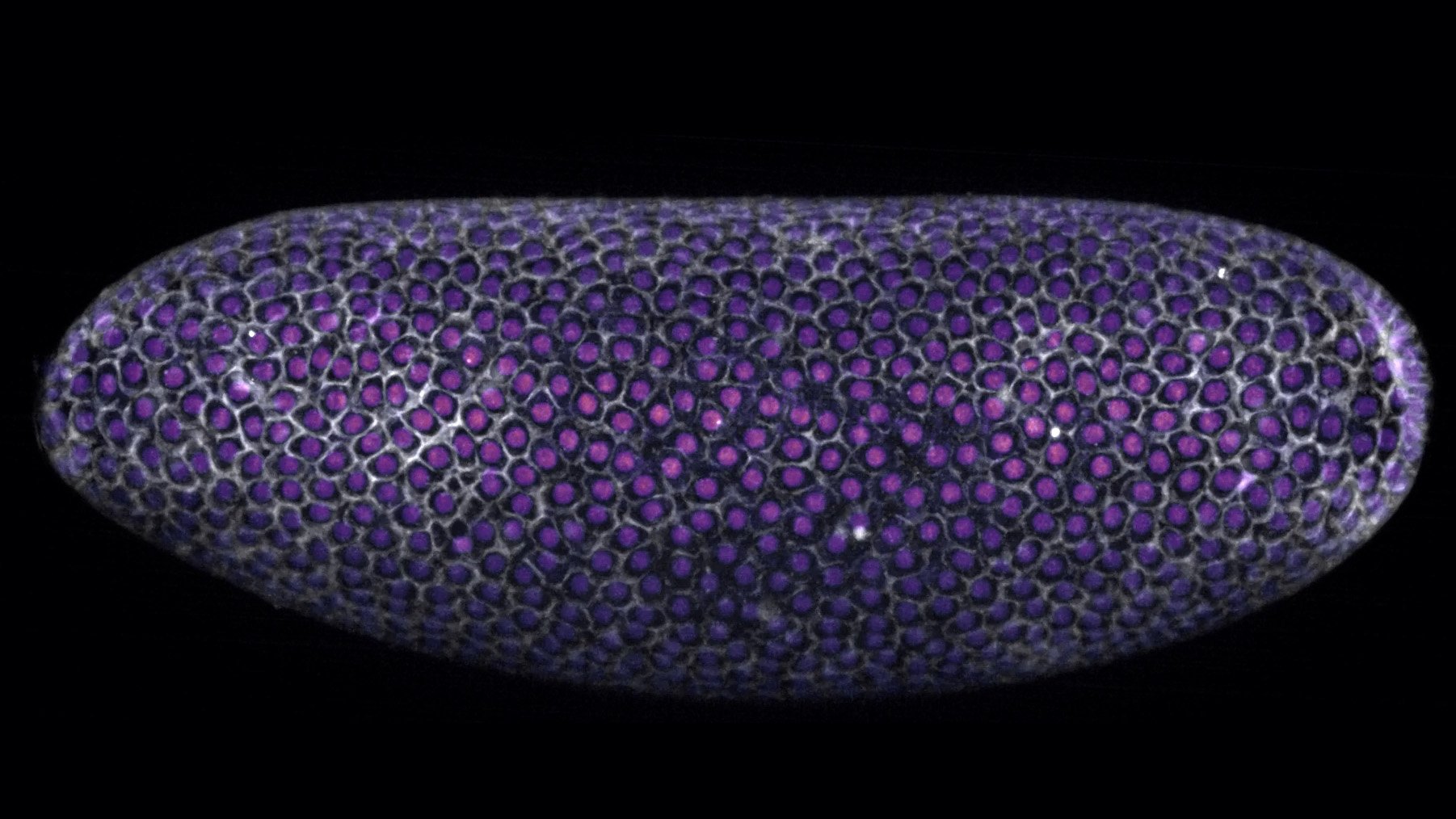
Naukowcy ze Szkoły Millera ujawniają mechanizmy stojące za ekspresją genów w mitochondriach
Przez: Cara Masset | 23 lipca 2024 r. | 6 min. czytania |
Udział
Podsumowanie artykułu
- Zespół badawczy Miller School jako pierwszy zmapował sposób, w jaki mitochondrialny mRNA składa się w komórkach ludzkich.
- Ekspresja DNA obejmuje jego transkrypcję do RNA, które następnie jest tłumaczone na białka zwane rybosomami.
- Praca ta definiuje kluczowy poziom regulacji ekspresji genów w mitochondriach i może pomóc w identyfikacji celów terapeutycznych w chorobach neurodegeneracyjnych.
Zespół badawczy zajmujący się biologią molekularną na Wydziale Medycznym Millera Uniwersytetu Miami jako pierwszy opracował mapę sposobu, w jaki mitochondrialny mRNA składa się w komórkach ludzkich.
Badania te poszerzają wiedzę na temat ekspresji genów w mitochondriach i otwierają drogę do identyfikacji celów terapeutycznych w leczeniu chorób neurodegeneracyjnych mitochondriów.
„Dysfunkcyjne mitochondria mogą powodować wyniszczające choroby, często rozpoczynające się w dzieciństwie, znane jako encefalomiopatie mitochondrialne. Pomimo postępów w identyfikacji genów odpowiedzialnych za te zaburzenia, ich mechanizmy patofizjologiczne są słabo poznane” — powiedział Antoni Barrientos, Ph.D., profesor neurologii, biochemii i biologii molekularnej w Miller School. „Było to częściowo spowodowane brakiem pełnego zrozumienia ekspresji genów mitochondrialnych. Konkretnie, nic nie było wiadome o tym, jak mitochondrialny mRNA się składa i jak może to wpływać na jego stabilność i translację w zdrowiu i chorobie”.
Teraz w artykule opublikowanym w numerze czasopisma z 19 lipca NaukaDr Barrientos i jego współautorzy ujawnili strukturom mitochondrialnego mRNA. Badania prowadzili dr Barrientos i Flavia Fontanesi, Ph.D., adiunkt biochemii i biologii molekularnej w Miller School, wraz z ich kolegą, Silvi Rouskin, Ph.D., adiunktem mikrobiologii w Harvard Medical School.
mRNA mitochondrialne
Mitochondria są jak maleńkie elektrownie wewnątrz ludzkich komórek. Przekształcają spożywane przez ludzi składniki odżywcze w energię, wykorzystując tlen do napędzania reakcji chemicznych. Ze względu na swoje bakteryjne pochodzenie, mitochondria zawierają małe, koliste DNA, które koduje 13 białek, które są składnikami enzymów wymaganych do transdukcji energii. Wszystkie inne białka mitochondrialne, do około 1500, są kodowane w DNA umieszczonym w jądrze, głównym repozytorium DNA komórki.
Ekspresja DNA obejmuje jego transkrypcję do RNA, które następnie jest tłumaczone na białka przez maszyny molekularne znane jako rybosomy. Wszystkie białka kodowane w jądrze są syntetyzowane w rybosomach zlokalizowanych w cytozolu komórki. 13 białek kodowanych w genomie mitochondrialnym jest syntetyzowanych w wyspecjalizowanych rybosomach zlokalizowanych w mitochondriach. W obu przypadkach rodzaj RNA znany jako informacyjny RNA (mRNA) przenosi instrukcje z DNA do rybosomów, aby wytwarzać białka.

Sposób, w jaki mRNA w jądrze się składa, jest krytyczny dla prawidłowego funkcjonowania komórki. Nieprawidłowo złożony mRNA powoduje lub przyczynia się do chorób neurologicznych i neurodegeneracyjnych. Jednakże składanie mRNA nigdy nie zostało zbadane w kontekście mitochondrialnych mRNA (mt-mRNA) i chorób mitochondrialnych.
Dr Barrientos i jego zespół rozwiązali problem fałdowania mt-mRNA podczas badań nad zespołem Leigha, genetyczną chorobą mitochondrialną powodującą degenerację określonych komórek w ośrodkowym układzie nerwowym.
„Chcieliśmy zbadać chorobę mitochondrialną znaną jako zespół Leigha, a konkretnie jej francusko-kanadyjską formę, która jest wynikiem mutacji w bogatym w leucynę białku zawierającym powtórzenia pentatrykopeptydowe (LRPPRC). LRPPRC, kodowany w genomie jądrowym, jest kluczowym regulatorem stabilności mt-mRNA i translacji na białka” — powiedział dr Barrientos. „Choroba jest wyniszczająca, ponieważ niemowlęta rzadko przeżywają drugi rok. Teraz odkryliśmy kilka podstawowych mechanizmów związanych z fałdowaniem mt-mRNA, które napędzają dziecięce choroby mitochondrialne, w tym zespół Leigha”.
Składanie mRNA
Aby rozpocząć prace nad likwidacją luki w wiedzy na temat fałdowania mt-mRNA, dr Barrientos i jego zespół zastosowali interdyscyplinarne podejście obejmujące badania nad ekspresją genów mitochondrialnych w zdrowiu i chorobie, opracowanie metod umożliwiających odczytanie struktur wszystkich mitochondrialnych mRNA, badania nad strukturą i funkcją oraz identyfikację potencjalnych celów terapeutycznych.
Zespół opracował metodę profilowania mutacji dimetylosiarczanu w mitochondriach z sekwencjonowaniem (mito DMS-MaPseq) i zastosował wykrywanie zespołów fałdowania RNA przy użyciu klasteryzacji maksymalizującej oczekiwania (DREEM), aby odkryć natywny krajobraz fałdowania lub strukturom mitochondrialnego informacyjnego RNA (mt-mRNA) w komórkach dzikiego typu i komórkach z niedoborem LRPPRC jako modelu zespołu Leigha.
Wyniki pomogły wyjaśnić rolę LRPPRC jako chaperonu holdase, który przyczynia się do utrzymania fałdowania mt-mRNA i wydajnej translacji. Ponadto, strukturalne spostrzeżenia mt-mRNA w mitochondriach dzikiego typu, w połączeniu z eksperymentami biochemicznymi, ujawniają szereg unikalnych mechanizmów regulacji translacji programowanej przez mRNA.
Mapy fałdowania mt-mRNA przedstawione w tej pracy stanowią podstawę do całościowego zrozumienia zależności pomiędzy strukturą mRNA a jego stabilnością, przetwarzaniem lub translacją.
Co dalej?
Praca zespołu otworzyła nowe kierunki badań naukowych.
„Dane w artykule definiują krytyczną warstwę regulacji ekspresji genów mitochondrialnych” – powiedział dr Fontanesi. „Te mapy fałdowania mt-mRNA stanowią punkt odniesienia do badania struktur mt-mRNA w różnych kontekstach fizjologicznych i patologicznych”.
Zespół kontynuuje badania nad tym, w jaki sposób struktura mRNA mt-mRNA dostosowuje się do różnych kontekstów komórkowych, stanów metabolicznych i warunków środowiskowych w zdrowiu i chorobach mitochondrialnych.
Dr Barrientos i dr Fontanesi wspólnie sprawowali opiekę nad J. Conorem Moranem, studentem studiów doktoranckich na Wydziale Biochemii i Biologii Molekularnej oraz pierwszym autorem badania, wraz z Amirem Brivanlou, studentem studiów podyplomowych w laboratorium dr Rouskin.
W Miami nad projektem pracowała i obecnie kontynuuje go dr Michele Brischigliaro, stażystka podoktorska w laboratorium dr Barrientos.
„Conor był siłą napędową projektu, łącząc biochemię wykonywaną w naszym laboratorium z procesami bioinformatycznymi opracowanymi w laboratorium dr. Rouskina na Harvardzie” — powiedział dr Fontanesi.
Tagi: biochemia i biologia molekularna, DNA, dr Antoni Barrientos, dr Flavia Fontanesi, mRNA