Rozplątanie wątków wczesnej demencji
-
Nauka odkrywcza
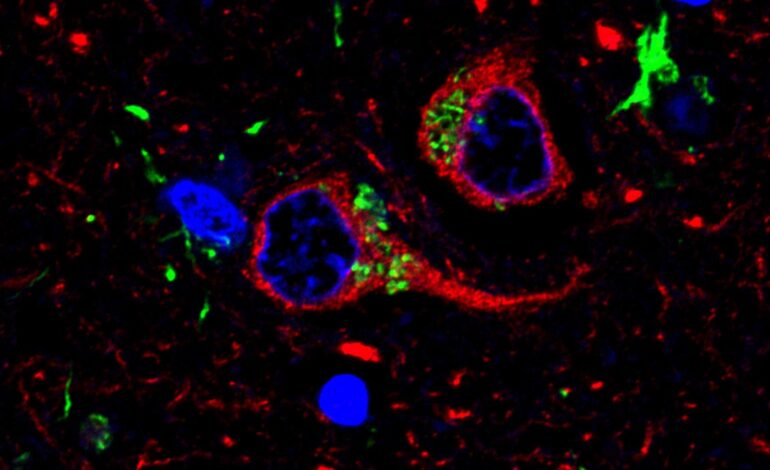
Zmiany osobowości, zachowania i języka są cechami charakterystycznymi otępienia czołowo-skroniowego (FTD), najczęstszej postaci demencji u pacjentów w wieku poniżej 65 lat, która jest związana ze zwyrodnieniem płatów czołowych i skroniowych mózgu. Naukowcy wiedzieli, że mniej powszechny ochronny wariant genu o nazwie TMEM106B może spowolnić postęp choroby, a teraz mają nowy wgląd w to, w jaki sposób części białka wytwarzane przez gen TMEM106B mogą zwiększać ryzyko i powodować przyspieszenie choroby.
Uważają, że klucz może leżeć w tworzeniu włókienek, czyli drobnych struktur przypominających włókna wytwarzanych przez część tego białka, które czasami splątują się w mózgu w wyniku nieznanego procesu. Naukowcy zaobserwowali, że u większości badanych osób z FTD struktury te kumulują się, natomiast u osób z formą ochronną są one praktycznie nieobecne. Badania mogą utorować drogę do lepszych metod leczenia w przyszłości.
O swoich odkryciach poinformowali w czasopiśmie Science Translational Medicine.
Dopiero niedawno społeczność badawcza odkryła, że białko TMEM106B tworzy w mózgu te nitkowate struktury.
Naukowcy z Mayo Clinic na Florydzie wraz ze współpracownikami postanowili ustalić powiązanie między strukturami TMEM106B, ochronnym wariantem genetycznym TMEM106B i FTD. Najpierw porównali czas trwania choroby u zmarłych pacjentów z FTD, którzy przekazali tkankę mózgową do banku mózgów Mayo Clinic. Odkryli, że osoby z wariantem ochronnym żyły średnio o trzy lata dłużej. Sugeruje to, że u tych pacjentów choroba postępowała wolniej.
Następnie stworzyli przeciwciało, które umożliwiłoby im wykrycie ilości struktur włóknistych w ludzkiej tkance mózgowej.
We wszystkich przypadkach FTD, które badacze przeanalizowali z banku mózgów – ponad 250 próbek – odkryli, że większość pacjentów miała stosunkowo wysoki poziom tych nitkowatych struktur w mózgach. Jednak te posiadające jedynie wariant ochronny TMEM106B miały niewiele lub nie miały go wcale. Stwierdzono dodatnią korelację między ilością struktur TMEM106B a poziomem innego patologicznego białka zwanego TDP-43, które jest silnie powiązane z FTD.

„Uderzające było to, że u osób z wariantem ochronnym nie doszło do gromadzenia się włókienek. Uważamy, że prawdopodobnie ma to coś wspólnego z tym, jak TMEM106B chroni przed FTD lub zmienia przebieg choroby, ale potrzeba więcej pracy, aby to zbadać ”, mówi Jordan Marks, doktor medycyny. student Mayo Clinic Graduate School of Biomedical Sciences i pierwszy autor artykułu. „Uważamy również, że te włókienka mogą pewnego dnia służyć jako biomarkery pomagające klinicystom w określaniu rokowania lub nasilenia FTD”.
Naukowcy twierdzą, że odkrycia mają konsekwencje dla przyszłych badań klinicznych.
„Nasze badania dostarczają dowodów na to, że warianty genetyczne w TMEM106B są istotnym czynnikiem, który należy wziąć pod uwagę w grupach badawczych pacjentów z FTD” – mówi dr Casey Cook, neurolog z Mayo Clinic i współautor artykułu do korespondencji. „Praca sugeruje również, że nowatorskie interwencje terapeutyczne zapobiegające gromadzeniu się splątanych struktur włóknistych mogą pewnego dnia zmniejszyć ryzyko choroby lub spowolnić jej postęp”.

Kolejne etapy badań zespołu obejmują walidację wyników w dodatkowych grupach pacjentów objętych badaniem oraz zbadanie sieci oddziałujących białek związanych z FTD, aby zapewnić dalszy wgląd w to, w jaki sposób nagromadzenie białka TMEM106B przyczynia się do choroby.
W powiązanym badaniu, opublikowanym również w Science Translational Medicine, badacze i współpracownicy Mayo Clinic odkryli nowe peptydy w mózgu i płynie mózgowo-rdzeniowym powstające, gdy TDP-43, również powiązany ze stwardnieniem zanikowym bocznym (ALS) lub chorobą Lou Gehriga, staje się dysfunkcyjny. Ich odkrycia mogą stanowić ramy dla opracowania testów klasy klinicznej do pomiaru patologii TDP-43 u żywych pacjentów.
Finansowanie badań nad TMEM106B zostało częściowo wsparte przez Narodowy Instytut Agingu Narodowego Instytutu Zdrowia, Narodowy Instytut Zaburzeń Neurologicznych i Udaru mózgu, Stowarzyszenie Alzheimera, ALLFTD, Fundusz Cure Alzheimer’s Fund, Centrum Badań nad Chorobą Alzheimera Mayo Clinic i Fundację Mayo Clinic. Pełną listę autorów i ujawnień można znaleźć w artykule.





