Śledzenie genetycznych przyczyn tocznia w celu personalizacji leczenia
Toczeń jest trwającą całe życie, często bolesną i czasami śmiertelną chorobą autoimmunologiczną. Obecnie istnieje niewiele metod leczenia poza silnymi sterydami osłabiającymi układ odpornościowy pacjenta – terapia niosąca ze sobą poważne ryzyko.
Dobra wiadomość jest taka, że nowe i obiecujące metody leczenia znajdują się w fazie badań klinicznych. Jednak termin toczeń zadaje kłam faktowi, że choroba ma wiele przyczyn, co oznacza, że leczenie będzie musiało być wysoce spersonalizowane, aby zagwarantować każdemu pacjentowi lek ukierunkowany na konkretną mutację genetyczną odpowiedzialną za odmianę tocznia, u której występuje.
Naukowcy dopiero teraz zaczynają łączyć określone mutacje genetyczne z podgrupami pacjentów z toczniem, umożliwiając lekarzom ukierunkowanie terapii na tych, którzy odniosą największe korzyści. W ramach najnowszego osiągnięcia naukowcy z Uniwersytetu Kalifornijskiego w Berkeley donoszą w nowym artykule o odkryciu dwóch grup pacjentów z mutacjami genetycznymi, które są niemal identyczne z mutacjami, które naukowcy wcześniej wskazali u myszy i linii komórkowych jako powiązane z chorobami autoimmunologicznymi. choroba.
Te dwa powiązania genetyczne należą do kilkudziesięciu mutacji, które zespół z Uniwersytetu Kalifornijskiego w Berkeley niedawno odkrył i powiązał z toczniem, a wszystko to w jednym genie regulującym głównego podejrzanego w podgrupie pacjentów z toczniem — białka zwane receptorami Toll-like (TLR), które umożliwiają układ odpornościowy komórki do rozpoznawania obcego DNA i RNA.
Według kierownika badania Gregory’ego Bartona, profesora biologii molekularnej i komórkowej na Uniwersytecie Kalifornijskim w Berkeley, identyfikacja tych mutacji może pomóc lekarzom w zapewnieniu spersonalizowanego leczenia pacjentów z nadwrażliwymi receptorami TLR, a w szczególności nadwrażliwymi receptorami TLR7.
To ekscytujące, ponieważ lek będzie dostępny doustnie i znajduje się obecnie w fazie badań klinicznych.
Wiktoria Rael, absolwentka
„W zasadzie mamy już mapę” – powiedział Barton, który jest także badaczem w Instytucie Medycznym Howarda Hughesa. „To nie jest tak, że każdy chory na toczeń ma mutację w genie powodującą nadmierną aktywację receptorów TLR i TLR7. Ale w Internecie pojawiają się leki, które bardzo specyficznie hamują TLR7. W miarę sekwencjonowania coraz większej liczby osób łatwiej będzie zidentyfikować tych pacjentów i przepisać im leki. To o wiele lepsze niż obecny sposób leczenia tocznia, który jest brutalny”.
„To ekscytujące, ponieważ lek będzie dostępny doustnie i znajduje się obecnie w fazie badań klinicznych” – powiedziała Victoria Rael, absolwentka Uniwersytetu Kalifornijskiego w Berkeley, która wraz z innym studentem Julianem Yano jest współautorem artykułu.
Wyniki badań genetycznych i szczegóły mutacji pacjentów opublikowano dzisiaj (23 maja) w czasopiśmie „ Journal of Experimental Medicine.
Problem z rozpoznaniem „siebie”
Choroby autoimmunologiczne, od reumatoidalnego zapalenia stawów i choroby Leśniowskiego-Crohna po twardzinę skóry i liczne choroby tarczycy, wynikają z ataków układu odpornościowego na własne komórki organizmu, które niszczą normalną, zdrową tkankę.
Victoria Rael i Gregory Barton z Uniwersytetu Kalifornijskiego w Berkeley
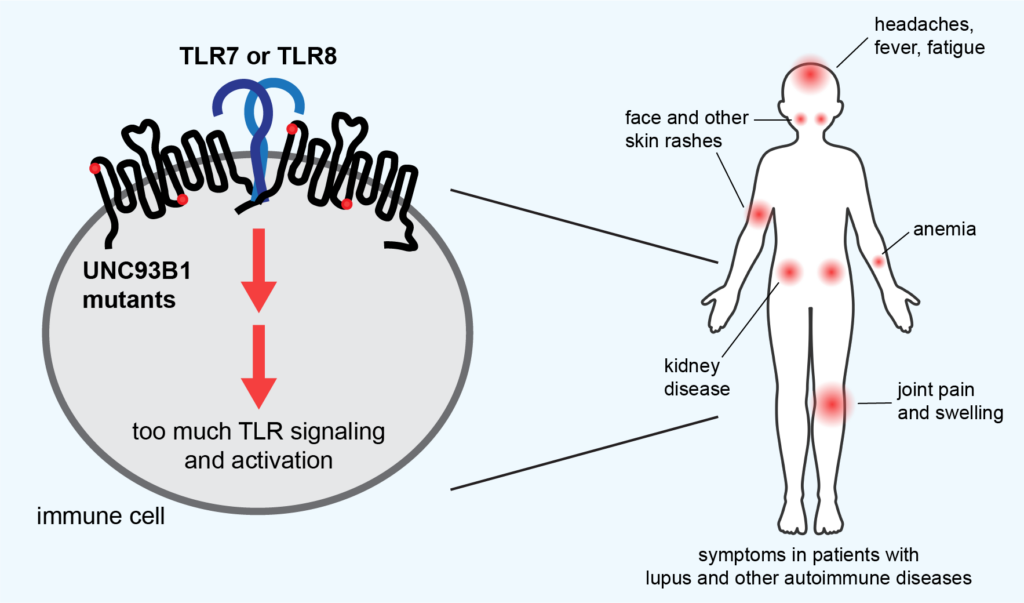
Wiele badań powiązało co najmniej dwa rodzaje chorób autoimmunologicznych, toczeń i łuszczycę, z receptorami TLR, które są częścią wrodzonego układu odpornościowego, który początkowo wykrywa obcych najeźdźców, takich jak wirusy i bakterie, i stymuluje pierwszą linię ataku. Zwykle receptory TLR są delikatnie dostrojone tak, aby reagować tylko na obce DNA i RNA, ale jeśli to dostrojenie jest wyłączone, mogą reagować na własne kwasy nukleinowe i białka związane z kwasami nukleinowymi, które wyglądają bardzo podobnie do patogenów.
To, co czyni tę reakcję autoimmunologiczną tak zabójczą, polega na tym, że receptory TLR aktywują także drugą linię obrony organizmu, silniejszą nabytą odpowiedź immunologiczną, mobilizującą limfocyty T i B, makrofagi i inne komórki. Komórki te następnie przeprowadzają ciągły atak, który niszczy zdrową tkankę organizmu i powoduje przewlekły stan zapalny.
Na przykład najczęstsza postać, toczeń rumieniowaty układowy (SLE), charakteryzuje się początkowo wysypką skórną – w szczególności wysypką w kształcie motyla na twarzy – ale później uszkodzeniem stawów, mięśni, narządów i skóry, powodującym ból i zmęczenie. Najczęściej występuje u kobiet, często zaczynając od nastoletnich lat. Ogólnie rzecz biorąc, toczeń występuje dwa do trzech razy częściej wśród kobiet z wielu grup mniejszości etnicznych i rasowych niż wśród białych kobiet.
…u niektórych osób receptor jest bardziej responsywny, więc teraz poziom własnych kwasów nukleinowych, który w przeciwnym razie nie stymulowałby receptora u normalnej osoby, aktywuje receptor.
Gregory Barton, profesor biologii molekularnej i komórkowej
„Uważamy, że system działa tak, że jeśli kwasy nukleinowe znajdą te receptory, najprawdopodobniej będą one pochodzić z wirusa” – powiedział Barton. „Ale u niektórych osób receptor jest bardziej responsywny, więc teraz poziom własnych kwasów nukleinowych, który w przeciwnym razie nie stymulowałby receptora u normalnej osoby, aktywuje receptor. Uważamy, że jednym ze sposobów działania tych mutacji jest wytwarzanie poziomów własnych kwasów nukleinowych, które normalnie nie byłyby stymulujące.
Barton i jego koledzy z laboratorium badali rolę receptorów TLR, które są błędnie regulowane w toczniu, a w szczególności jednego z głównych białek, które je regulują: UNC93B1, w skrócie UNC. Kilka lat temu zespół doktorantów i doktorantów w jego laboratorium przebadał w hodowli komórkowej ponad 100 mutacji genetycznych w genie UNC, aby sprawdzić, które z nich powodują nadmierną stymulację receptorów TLR i będą dobrymi celami dalszych badań. Chociaż opublikowali pewne szczegóły we wcześniejszych artykułach, nie opublikowali pełnej listy, ponieważ wydawało się, że nie ma to większego sensu — prawie nie było dostępnych danych na temat sekwencji genomu pacjentów z toczniem, które można by porównać z mutacjami, które nadmiernie stymulują receptory TLR.
To się jednak zmieniło w ostatnich latach dzięki gwałtownym spadkom kosztów sekwencjonowania genomu. Tak odnalazła Bartona matka młodej dziewczynki chorej na ciężką chorobę autoimmunologiczną. DNA jej córki zostało zsekwencjonowane i wykazało mutację w regionie UNC, którą zespół Bartona zauważył we wcześniejszej pracy.
Toczeń w rodzinie
Rael i studentka Madeleine Weiss zastosowali tę samą technikę badań przesiewowych hodowli komórkowych, aby przetestować nową mutację młodej dziewczyny i odkryli, że ma ona działanie nadmiernie stymulujące, podobne do efektu innych mutacji w tym obszarze genu UNC. Co zaskakujące, pacjentka miała mutację genetyczną tylko w jednym z dwóch alleli UNC, co oznacza, że miała jeden prawidłowy gen UNC, a mimo to nadal cierpiała na poważne objawy autoimmunologiczne.

Dzięki uprzejmości Amerykańskich Centrów Kontroli i Zapobiegania Chorobom
Barton i jego zespół nawiązali także kontakt z pięcioosobową rodziną dotkniętą toczniem. Wszyscy mieli mutacje na jednym allelu UNC w innym obszarze białka UNC, który zespół Bartona wcześniej zidentyfikował. Mutacja ta, poddana badaniu przesiewowemu w liniach komórkowych, również wytworzyła nadaktywne receptory TLR.
„Byliśmy sceptyczni, czy tylko jedna kopia genu wystarczy, aby wywołać chorobę” – powiedział Rael. „Dopiero gdy umieściliśmy mutacje pacjentów w liniach komórkowych i zobaczyliśmy, że prowadzą one do bardzo przekonującej nadreaktywności receptorów TLR, zdaliśmy sobie sprawę, że mogą one być wystarczające, aby wywołać chorobę”.
Następnie Rael i Yano powtórzyli badania przesiewowe przeprowadzone wcześniej w laboratorium i potwierdzili, że 32 różne mutacje w genie UNC — około jedna trzecia przetestowanych mutacji — zwiększyły wrażliwość TLR7 na kwasy nukleinowe co najmniej dwukrotnie. Około pięciu kolejnych mutantów zwiększyło czułość TLR7, ale w mniejszym stopniu. Przed tymi badaniami tylko dwie mutacje w białku UNC powiązano ze zwiększoną wrażliwością TLR7 u myszy, chociaż w ciągu ostatnich dwóch miesięcy zgłoszono trzy dodatkowe mutacje u ludzi.
Barton ma nadzieję, że publikując pełną listę mutacji związanych z nadwrażliwością TLR, lekarze będą mogli zidentyfikować innych pacjentów z toczniem, którzy mogliby odnieść korzyść ze stosowania leków anty-TLR znajdujących się obecnie w badaniach klinicznych. Wydaje się, że jeden z leków, M5049 lub Enpatoran, działa poprzez przyczepianie się do dwóch ludzkich receptorów, TLR7 i TLR8, i uniemożliwianie im wiązania kwasów nukleinowych.
Rael, Yano i inni członkowie laboratorium Bartona badają dalej, w jaki sposób te unikalne mutacje UNC wpływają na sposób, w jaki pacjent objawia się chorobą. Odtworzyli mutacje tych pacjentów u myszy, aby móc modelować ludzki toczeń.
„Dzięki modelom mysim można zacząć zastanawiać się, w jaki sposób – mimo że mutacje występują w tym samym białku – załamują się różne mechanizmy regulacji TLR, które komórki odpornościowe zostają w rezultacie aktywowane i jak może to prowadzić do różnic w objawach” cierpią pacjenci” – powiedział Rael.
Laboratorium próbuje także zrozumieć, w jaki sposób UNC dostraja receptory TLR, co może odbywać się poprzez regulację liczby i rozmieszczenia receptorów TLR na komórkach odpornościowych. Więcej TLR może sprawić, że dana osoba będzie bardziej wrażliwa na niewielką liczbę własnych kwasów nukleinowych krążących w organizmie.
„UNC93B1 jest ważny, aby doprowadzić receptory do miejsca, w którym mogą funkcjonować, ale jest również ważny dla regulowania ich, kiedy już tam dotrą” – powiedział Barton. „Białko to bardzo barokowy sposób podejmowania decyzji, czy kwas nukleinowy, który właśnie związałeś z TLR, pochodzi z wirusa, czy z jednej z twoich własnych komórek”.
Ma nadzieję, że lekarze dodadzą ten gen do listy genów związanych z toczniem, „więc jeśli zobaczą taką mutację, nawet heterozygotyczną, będą badać dalej”.
Innymi starszymi autorami artykułu są Bo Liu z Chińskiej Akademii Nauk w Szanghaju i Olivia Majer z Instytutu Biologii Zakażeń Maxa Plancka w Berlinie w Niemczech. Współautorami są także lekarze z Uniwersytetu Kalifornijskiego w San Francisco, Uniwersytetu Stanforda oraz szpitali w Missouri, Karolinie Północnej i Waszyngtonie.
Prace zostały częściowo sfinansowane przez Lupus Research Alliance, dawniej Instytut Badań nad Lupusem, oraz National Institutes of Health (R01AI072429).
POWIĄZANA INFORMACJA






