Zespół Dubina-Johnsona u bliźniaków powiązany z listopadem
obraz:
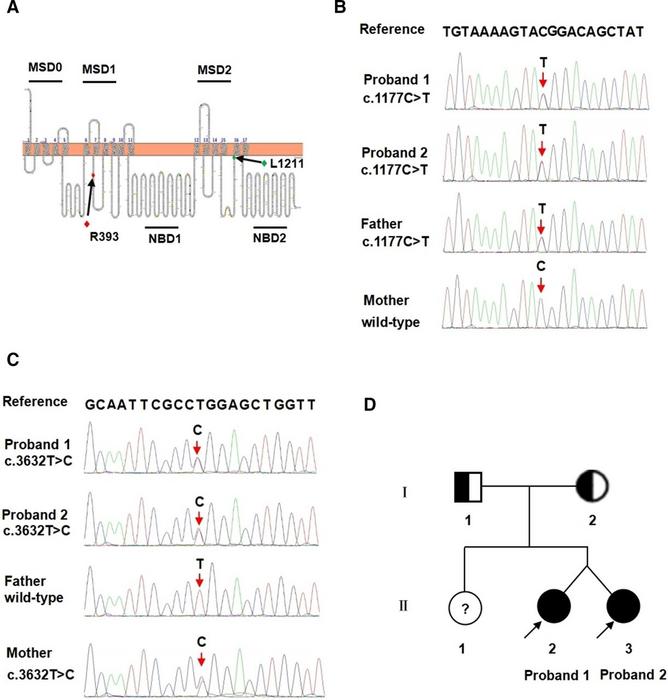
(A) Lokalizacja R393 i L1211 w przewidywanym modelu topologii białka MRP2. Pełnowymiarowy model wygenerowano za pomocą narzędzia Protter o otwartym kodzie źródłowym ((B) Analiza sekwencjonowania pliku ABCC2 gen wskazuje na związany z chorobą wariant probantów (II-2, II-3), mutacja zmiany sensu 1177C>T, która przewidywana jest jako powodująca mutację Arg393Trp (R393W) w sekwencji aminokwasowej białka MRP2 dziedziczonego od ojca (I -1) i (C) mutacja zmiany sensu 3632T>C (L1211P) odziedziczona od matki (I-2). (D) Rodowód przedstawiającej się rodziny ABCC2 warianty. Koła i kwadraty reprezentują odpowiednio kobiety i mężczyzn. Symbole wypełnione w połowie czarnym kolorem reprezentują heterozygotycznych nosicieli mutacji, a symbol znaku zapytania wskazuje normalnego osobnika bez badania genetycznego. Symbole wypełnione czarnym kolorem przedstawiają bliźniaczych probantów. MSD, domena rozciągająca się przez błonę; NBD, domena wiążąca nukleotydy.
pogląd więcej
Źródło: Sun R, Chen Y, Zhu M i in.
Naukowcy z Chin i Włoch dokonali znaczącego przełomu w zrozumieniu zespołu Dubina-Johnsona (DJS), rzadkiej dziedzicznej choroby wątroby. Zespół zidentyfikował konkretne mutacje genetyczne odpowiedzialne za DJS u pary bliźniąt dwuzygotycznych, dostarczając cennych informacji na temat przyczyny choroby i potencjalnie poprawiając diagnozę pacjentów z niejasnymi objawami.
DJS zakłóca zdolność wątroby do usuwania produktów przemiany materii, co prowadzi do gromadzenia się bilirubiny, żółtego pigmentu we krwi. Może to powodować żółtaczkę – stan charakteryzujący się zażółceniem skóry i białek oczu. Jednak objawy DJS są często łagodne i łatwe do przeoczenia, co utrudnia rozpoznanie.
Badanie opublikowane w eGastroenterologia, wykorzystali sekwencjonowanie całego egzomu (WES), potężną technikę analizy genetycznej. Projekt WES umożliwił naukowcom zbadanie regionów kodujących białka wszystkich ludzkich genów w DNA bliźniąt. Ta szczegółowa analiza ujawniła dwie krytyczne mutacje w genie ABCC2 gen, który dostarcza instrukcji budowy białka zwanego MRP2. MRP2 pełni rolę transportera, eliminując produkty przemiany materii z komórek wątroby.
Wcześniej zgłaszano, że jedna ze zidentyfikowanych mutacji jest powiązana z DJS. Mutacja ta znacząco zmniejsza ogólną ilość białka MRP2 wytwarzanego przez komórki wątroby.
Zespół badawczy odkrył także nową mutację w genie ABCC2 gen, niepowiązany wcześniej z DJS. Ta nowo zidentyfikowana mutacja zmienia samo białko MRP2, utrudniając jego zdolność do prawidłowego funkcjonowania na błonie komórkowej.
Uważa się, że łączny efekt tych mutacji zakłóca normalny przepływ produktów przemiany materii z komórek wątroby. Uważa się, że to upośledzony system przetwarzania odpadów jest podstawową przyczyną DJS u tych bliźniaków.
Badanie podkreśla skuteczność WES w diagnozowaniu DJS, szczególnie u pacjentów z nietypowymi objawami lub łagodnymi objawami. Tradycyjnie diagnozowanie DJS opierało się na objawach klinicznych, biopsjach wątroby i określonych badaniach. Jednak metody te nie zawsze mogą być rozstrzygające, zwłaszcza we wczesnych stadiach choroby.
WES oferuje bardziej precyzyjne i obiektywne podejście do diagnozowania DJS. Identyfikując konkretne mutacje genetyczne odpowiedzialne za tę chorobę, lekarze będą mogli pewnie diagnozować pacjentów i kierować ich przyszłym leczeniem.
Chociaż badanie to skupiało się na pojedynczym przypadku dotyczącym bliźniąt, jego ustalenia mają szersze implikacje. Naukowcy uważają, że mutacje te mogą występować u innych osób, u których zdiagnozowano DJS, co potencjalnie wyjaśnia pewną zmienność w obserwowanym nasileniu choroby. Aby potwierdzić te wstępne ustalenia, konieczne są dalsze badania z udziałem większej populacji pacjentów.
To badanie jest kluczowym krokiem naprzód w odkrywaniu tajemnic DJS. Wyjaśniając podłoże genetyczne choroby, torujemy drogę do lepszej diagnostyki, co potencjalnie może prowadzić do opracowania nowych strategii leczenia w przyszłości.
Zespół badawczy bada obecnie długoterminowe konsekwencje zdrowotne tych mutacji i ich potencjalny wpływ na czynność wątroby. Współpracują także z innymi badaczami, aby przeprowadzić większe badania w celu potwierdzenia swoich wyników i zbadania potencjalnych opcji terapeutycznych dla pacjentów z DJS.
Zobacz artykuł:
Sun RY, Chen YM, Zhu MM, i in. ABCC2 Wariant p.R393W przyczynia się do zespołu Dubina-Johnsona poprzez ukierunkowanie MRP2 na degradację proteasomu. eGastroenterologia 2024;2:e100039. doi:10.1136/egastro-2023-100039
O eGastroenterologia
eGastroenterologia to nowe, ogólnodostępne i recenzowane czasopismo BMJ, które koncentruje się na badaniach medycyny podstawowej, klinicznej, translacyjnej i opartej na dowodach we wszystkich obszarach gastroenterologii (w tym hepatologii, pankreatologii, esofagologii i chirurgii przewodu pokarmowego).
Aby uzyskać więcej informacji prosimy odwiedzić: egastroenterology.bmj.com i śledź nas dalej Świergot (@eGastro_BMJ).
Zarejestruj się, aby otrzymywać powiadomienia e-mail dotyczące eGastroenterologii:
Dziennik
eGastroenterologia
Tytuł artykułu
Wariant ABCC2 p.R393W przyczynia się do zespołu Dubina-Johnsona poprzez ukierunkowanie MRP2 na degradację proteasomu
Zastrzeżenie: AAAS i EurekAlert! nie odpowiadają za dokładność komunikatów prasowych publikowanych w EurekAlert! przez instytucje wnoszące wkład lub za wykorzystanie jakichkolwiek informacji za pośrednictwem systemu EurekAlert.






